Donanemab是由美国礼来公司研发的抗β淀粉样蛋白(Aβ)药物,于2024年7月获美国FDA批准上市(KISUNLA® Donanemab),用于治疗阿尔茨海默病(AD)。
目前Donanemab在国内尚未获批,中文名暂译为多奈尼单抗(音译无出处)。
1、作用机制
阿尔茨海默病(Alzheimer’s disease; AD),俗称老年痴呆,是一种发病进程缓慢、随时间不断恶化的神经退化性疾病。
传统AD治疗药物
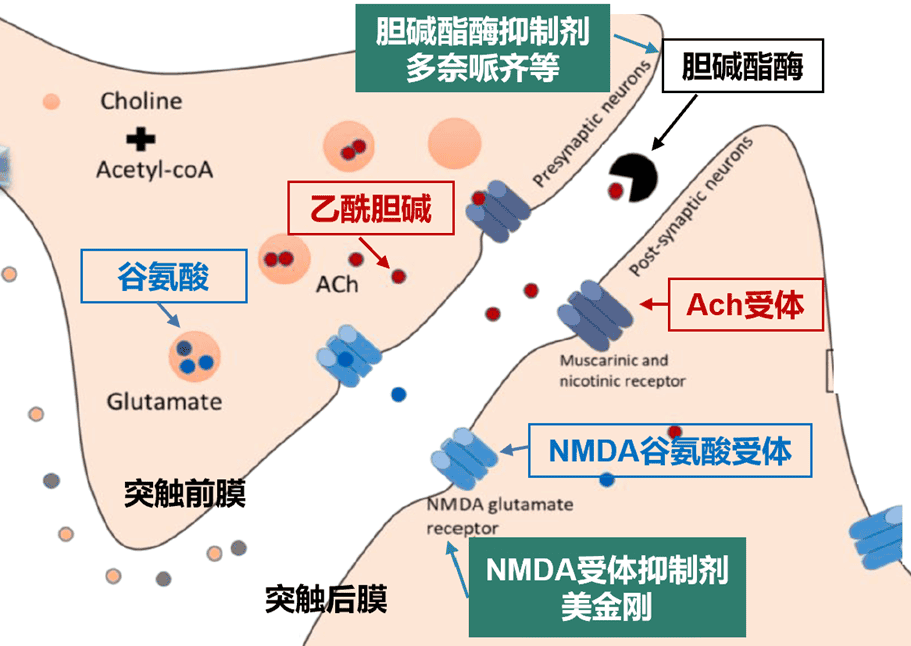
1、胆碱酯酶抑制剂:
依据胆碱能假说,AD患者胆碱能神经传递功能降低。
胆碱酯酶抑制剂(AChEI)可通过减少乙酰胆碱的水解而增加突触间隙中乙酰胆碱(ACh)的浓度,增加AD患者胆碱能神经传递功能,缓解阿尔茨海默病症状。
常规治疗药物包括:多奈哌齐,加兰他敏,利斯的明等。
2、NMDA谷氨酸受体抑制剂:
与AD患者ACh神经功能低下相反,NMDA受体过度激活在AD中的毒性作用目前已经得到证实。
美金刚是一种非竞争性NMDA受体拮抗剂,通过阻断NMDA受体的过度激活,减少谷氨酸诱导的神经毒性,保护神经元,减缓阿尔茨海默病的症状进展。
无论是胆碱酯酶抑制剂,还是NMDA谷氨酸受体抑制剂,目前均仅能缓解症状,不能从根本上逆转AD。
现代AD治疗药物
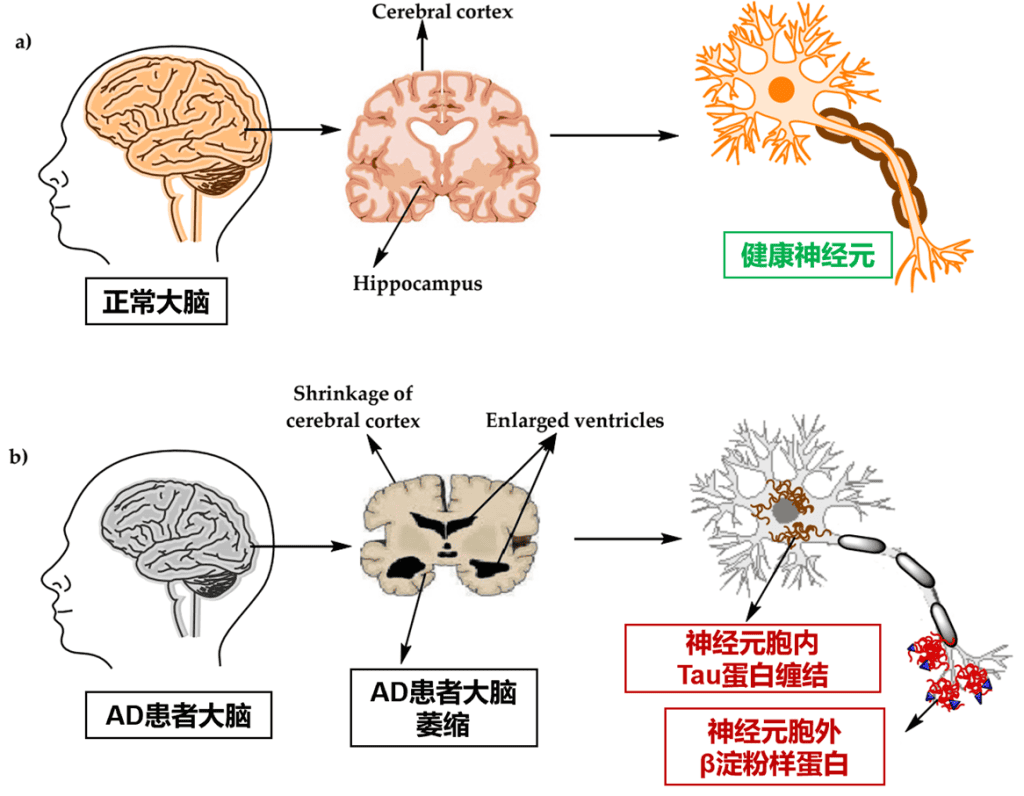
目前较流行的阿尔茨海默病AD发病机制假说主要包括Tau蛋白假说,β淀粉样蛋白级联假说。
1、β淀粉样蛋白级联假说:
目前最经典的AD发病机制学说,认为β淀粉样蛋白(Aβ)在神经元胞外过度沉积,在患者大脑皮层形成老年斑,导致病理生理改变。
淀粉样前体蛋白(APP)在人体内合成后,通过β和γ分泌酶的剪切进行代谢。
随着年龄的增长或分泌酶功能异常,APP代谢生成的Aβ增多,导致其在神经元胞外沉积。这一过程经历Aβ42单体、Aβ42寡聚体、Aβ斑块形成,最终形成神经元胞外沉积。
2、Tau蛋白假说:
神经元胞内,Tau蛋白纤维缠结是AD的第二大病理表现。Tau蛋白过度磷酸化导致正常的微管解聚,随后导致细胞出现树突微管丢失,突触功能障碍,直至细胞死亡。
虽然目前还没有上市的Tau蛋白靶向治疗药物,但这种机制是未来阿尔茨海默病治疗的一个重要研究方向。
β淀粉样蛋白为靶点的药物
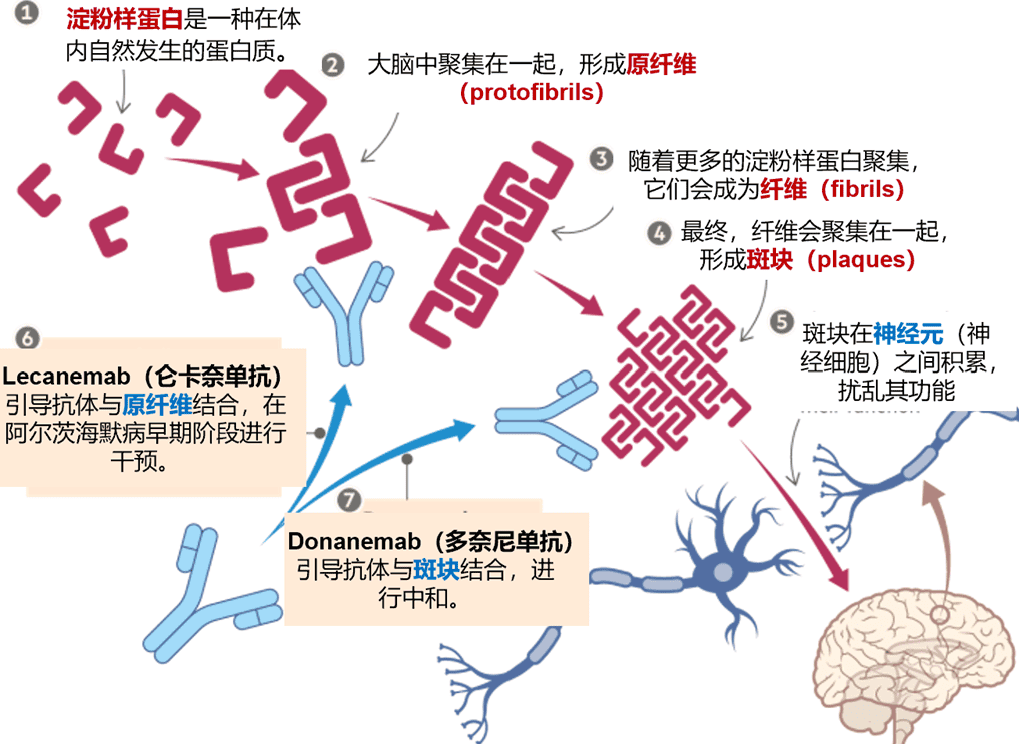
以β淀粉样蛋白为靶点,目前FDA已经获批的生物制剂有3款:
1、Aducanumab(阿杜卡单抗)
Aducanumab是渤健公司和卫材公司联合开发的,用于治疗AD的药物。由于药物上市后争议不断,卫材公司已退还Aducanumab的权益,集中资源研发另一个AD药物Lecanemab(仑卡奈单抗)。
Aducanumab的临床实验主要终点选取了 β 淀粉样蛋白降低的替代终点,而非认知功能提高的“硬终点”,并且替代终点的效果也不理想。
2020年FDA召开专家咨询委员会讨论Aducanumab的上市请求,10人专家组8人反对,2人弃权。但是FDA力排众议,与2021年批准该药上市(ADUHELM® aducanumab)。
2、Lecanemab(仑卡奈单抗)
卫材公司放弃Aducanumab后,将主要精力放在了Lecanemab上。
该药物在一项为期18个月的安慰剂对照III期临床研究(Clarity AD)中,主要研究终点为临床痴呆评定量表总评分(CDR-SB)较基线变化。研究结果达到显著统计学差异(P<0.001),相较于安慰剂组,Lecanemab治疗组的认知衰退幅度减缓了27%。
基于以上硬终点数据,FDA于2023年1月批准Lecanemab上市(LEQEMBI® lecanemab)。
2024年1月药物获得中国药监局批准上市(乐意保® 仑卡奈单抗)。
3、Donanemab(多奈尼单抗)
礼来公司的Donanemab是第三款上市的β淀粉样蛋白抑制剂。于2024年7月获得美国FDA批准上市(KISUNLA® Donanemab)
根据礼来公司公布了为期6个月的头对头III期临床研究(TRAILBLAZER-ALZ 4)数据。与安慰剂组相比,Donanemab组患者的临床痴呆评定量表总评分(CDR-SB)降低减缓了29%。
2、适应症
3款FDA批准阿尔兹海默病药物
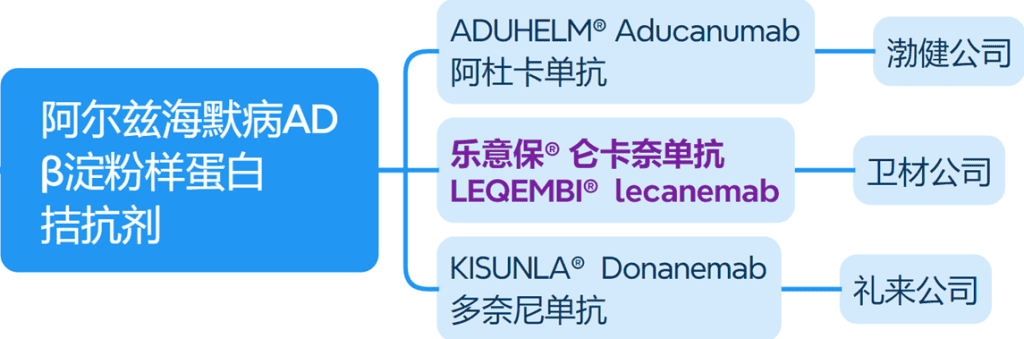
目前FDA已经获批的3款以β淀粉样蛋白为靶点的阿尔兹海默病(AD)药物为:
ADUHELM® Aducanumab 阿杜卡单抗 – 渤健公司
LEQEMBI® lecanemab 乐意保® 仑卡奈单抗 – 卫材公司
KISUNLA® Donanemab 多奈尼单抗 – 礼来公司
3、图像记忆

卡车上的一袋淀粉,代表药物靶点β淀粉样蛋白。
破碎的头像,代表老年痴呆患者,阿尔兹海默病。
阿杜开着卡车代表阿杜卡单抗。
轮子卡住,代表仑卡奈单抗。
很多声纳尼,代表多奈尼单抗。
你记住了么


牛13